Autor: Željko Vojvodić, dr. med.
Ordinacija obiteljske medicine Bijelo brdo
Početak primjene antibiotika kao temeljnog načela liječenja infektivnih bolesti označio je promjenu koju je malo tko tada mogao predvidjeti. Pored učinka na produljenje očekivanog trajanja života dramatičnim smanjenjem smrtnosti od dječjih infektivnih bolesti (zajedno s imunizacijama), njihova pojava potaknula je niz promjena u medicinskoj struci koje su znatno pridonijele općem civilizacijskom napretku. Promijenio se cjelokupni pogled na svijet kako među pripadnicima medicinske struke tako i šire javnosti te se danas osjećamo mnogo sigurnije i imamo mnogo više pouzdanja u medicinu nego što su imali prije samo tri generacije. Prva desetljeća upotrebe bila su obilježena entuzijazmom: pojava novih antibiotika smatrala se gotovo normalnom, a nove skupine obilježavale su svako desetljeće.
Porast zanimanja za antibiotike starije generacije započinje početkom 2000-ih godina kada je postalo jasno da antibiotici širokog spektra ne mogu suzbiti antimikrobnu rezistenciju odnosno učinkovito liječiti, već su naprotiv vrlo aktivni i vrlo potentni promotori bakterijske rezistencije u smislu pojačanog selekcijskog pritiska. Peroralni cefalosporini počeli su se primjenjivati početkom 1970-ih (cefaleksin, 1970.), gotovo istodobno kao i kombinacija sulfametoksazol-trimetoprima (kotrimoksazola), 1970. Peroralni cefalosporini druge generacije pojavljuju se u 1980-im, fluorokinoloni (ciprofloksacin) u drugoj polovini 1980-ih. Za liječenje mokraćnih infekcija u primarnoj zdravstvenoj zaštiti postupno su se izdvojila dva antibiotika: nitrofurantoin i fosfomicin, zbog stabilne učinkovitosti tijekom desetljeća u upotrebi i u okolnostima rastuće rezistencije. Njima je 2011. pridodan i trimetoprim, odnosno kotrimoksazol, sa zadovoljavajućom učinkovitošću u sredinama s razinom rezistencije E. coli ispod 20 %. Opravdanost primjene samo triju antibiotika u nekompliciranom cistitisu, kao i znanstvena i stručna utemeljenost ovih preporuka, detaljno je elaborirana u smjernicama američkog Infektološkog društva (IDSA) 2011. Zanimljivo je napomenuti kako su u švedskim antimikrobnim smjernicama za nekomplicirani cistitis nitrofurantoin i fosfomicin preporučeni još 2007., dakle prije objavljivanja IDSA-inih smjernica i što je još važnije – uz izostanak cefalosporina i fluorokinolona. Ove preporuke, uz neznatne izmjene i nadopune, vrijede i danas unatoč činjenici da je rezistencija znatno proširenija nego prije 10 godina i unatoč tome što se višestruko rezistentni uzročnici gotovo rutinski izoliraju u izvanbolničkoj sredini, podjednako kao i u bolnicama.
Rezistencija je bila na puno manjoj razini nego danas. Sojevi E. coli koji produciraju beta-laktamaze proširenog spektra (ESBL – en. extended spectrum beta-lactamases) opisani su prvi put u literaturi 1979. Beta-laktamaze proširenog spektra, kao zasebna skupina, hidroliziraju (cijepaju) sve beta-laktamske antibiotike, uključujući cefalosporine proširenog spektra. Od sredine 1980-ih godina prošlog stojeća njihova prevalencija raste, isprva u većim bolničkim centrima, a kasnije i u izvanbolničkoj sredini. Dijele se prema opsegu i vrsti aminokiselinskih supstitucija u fenotipske klastere: TEM i SHV (klasa A) užeg su spektra, dok je danas najrasprostranjeniji tip među gram-negativnim organizmima CTX-M, s puno širim spektrom inaktivacije antibiotika. Budući da su geni koji ih kodiraju smješteni na plazmidima, prijenos i širenje u mikrosredini odvija se puno brže nego prilikom spontanih mutacija. Do danas je opisano oko 160 podtipova u skupini CTX M, a ona danas čini dominantni fenotip među rezistentnim sojevima E. coli i drugih enterobakterija.
Slika 1 pokazuje kronološki slijed otkrića i početka primjene pojedinih beta-laktamskih antibiotika i nastanak novih generacija beta-laktamaza koje ih razaraju. Autor članka nimalo slučajno naziva ovaj slijed događaja velikim ratom između bakterija i čovjeka [1].
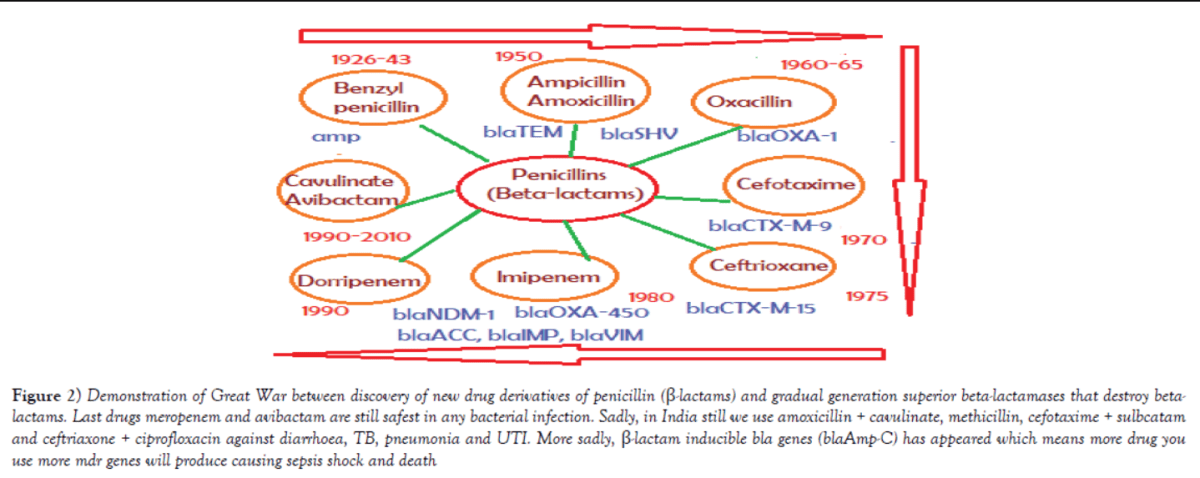
Čime ćemo, dakle, liječiti mokraćne infekcije u bližoj budućnosti? Odgovor je: istim onim lijekovima koje koristimo i danas zato što drugih nema. Peroralni cefalosporini i fluorokinoloni postajat će sve manje pouzdani, dok će antibiotici prve linije vjerojatno zadržati zadovoljavajuću terapijsku učinkovitost, ali uz dva uvjeta. Prvo, štedljivo propisivanje, odnosno pažljivo i detaljno procjenjivanje postoji li uopće potreba za njihovom primjenom u svakom pojedinom slučaju. Najčešća je pogreška primjena pri kolonizaciji (asimptomatskoj bakteriuriji), nasuprot simptomatskoj infekciji, u pacijenata bez komplicirajućih čimbenika jer kolonizaciju ne treba liječiti. Kao drugo, važno je ispravno doziranje. Ispravno doziranje omogućuje ne samo optimalnu učinkovitost i u nekompliciranim i u kompliciranim (ponavljajućim i rezistentnim) infekcijama, već isto tako osigurava eradikaciju uzročnika, neovisno o tome radi li se o osjetljivim ili višestruko rezistentnim sojevima.
Liječenje pacijenata u primarnoj zdravstvenoj zaštiti sve je više opterećeno poteškoćama oko razlučivanja nekompliciranih i kompliciranih slučajeva zbog porasta rezistencije gram-negativnih uzročnika u izvanbolničkoj sredini i nedostatka pouzdanih peroralnih alternativa antibioticima prve linije (nitrofurantoin, fosfomicin, kotrimoksazol). Na enterobakterije koje proizvode CTX beta-laktamaze proširenog spektra, i koje se sve češće izoliraju u izvanbolničkoj sredini, ne djeluju aminopenicilini, amoksicilin s klavulanatom, svi peroralni i parenteralni cefalosporini, aminoglikozidi, trimetoprim-sulfametoksazol i svi fluorokinoloni. Time se spektar učinkovitih antibiotika smanjuje na praktički samo dva: fosfomicin i nitrofurantoin, koji za sada dobro djeluju na rezistentne sojeve. Ukrižena rezistencija na više skupina antibiotika posebno je karakteristična za uzročnike urinarnih infekcija i sve se učestalije susreće u pacijenata u skrbi liječnika obiteljske medicine širom svijeta, i to u rizičnim skupinama (dijabetičari, kronični srčani i bubrežni bolesnici, pacijenti s opstruktivnim uropatijama, urolitijazom i sl.), kao i među pacijentima bez jasno prepoznatljivih rizičnih čimbenika. Među gram-pozitivnim uzročnicima mokraćnih infekcija u porastu je rezistencija enterokoka (vankomicin-rezistentni enterokoki, VRE), koji se najčešće izoliraju u kateteriziranih pacijenata te su ove infekcije karakteristične za bolničke ustanove. No, budući da se primjena katetera sve više obavlja u kućnim uvjetima, domovima za starije i udomiteljskim obiteljima, za očekivati je da će razina rezistentnih izolata porasti i izvan bolnica. I fosfomicin i nitrofurantoin imaju izvrstan učinak na enterokok rezistentan na vankomicin. Enterokoki su inače dio normalne flore gastrointestinalnog trakta i oko 95 % svih izolata u fecesu čini E. faecalis, koji je u pravilu osjetljiv na vankomicin i tradicionalni antienterokokni lijek amoksicilin (VSE – vancomycin-sensitive Enterococcus). Većinu VRE-a čini E. faecium. Porast prevalencije VRE-a nastao je zbog selekcijskog pritiska uzrokovanog ekstenzivnom upotrebom vankomicina (odobren 1958.). Od 1980. pa tijekom sljedeća dva desetljeća zabilježen je dramatičan porast kliničke primjene od 100 puta [2].
FOSFOMICIN
Po kemijskoj strukturi ne pripada nijednoj klasi antibiotika (epoksid fosfonične kiseline). Inhibira sintezu staničnog zida (peptidoglikana) u ranom stadiju. U bakterijske stanice ulazi aktivnim transportom (uptake) preko alfa-glicerofosfatnog i heksoza-fosfatnog transportnog sustava. Unutar bakterije kompetitivno inhibira enolpiruvil transferazu (natječe se s fosfoenolpiruvatom) u prvom koraku sinteze peptidoglikana. Budući da je inhibicija enzima ireverzibilna, sinteza staničnog zida potpuno se prekida i bakterija ugiba zbog osmotske neravnoteže. Na aktivno umnažajuće bakterije djeluje baktericidno. Spektar obuhvaća gram-pozitivne koke (enterokok osjetljiv na vankomicin i enterokok rezistentan na vankomicin), H. influenzae, E. coli, Proteus spp. (na koji nitrofurantoin ne djeluje), Salmonella spp., Shigella spp. Nema učinak na Pseudomonas. Rezultati in vitro testiranja ne koreliraju pouzdano s kliničkom učinkovitošću zbog nedostatka standardiziranih testova osjetljivosti (osim prema E. coli i E. faecalis). Unatoč širokom antibakterijskom spektru, odobren je samo za liječenje nekompliciranog cistitisa u žena iznad 12 godina. U SAD-u (FDA) odobren je za liječenje nekompliciranih mokraćnih infekcija uzrokovanih bakterijama E. coli i E. faecalis, kao i kompliciranih cistitisa bez bakterijemije. Kontraindiciran je kod sumnje na pijelonefritis ili perinefritički apsces. Postoji i parenteralni pripravak za liječenje ozbiljnih višestruko rezistentnih infekcija unutarnjih organa.
Sustavni pregled publikacija između 1987. i 1999. potvrdio je podjednaku kliničku i mikrobiološku učinkovitost fosfomicina u usporedbi s komparatorima (kinoloni, trimetoprim, beta-laktami, nitrofurantoin). Ukupno je obuhvaćeno 1657 pacijenata, pretežno žena s nekompliciranim cistitisom [3]. U nekoliko studija s uključivanjem muških pacijenata i djece, fosfomicin je pokazao ponovno podjednaku učinkovitost s komparatorima. U većini antimikrobnih smjernica pa tako i našim smjernicama ISKRA za dijagnozu i liječenje mokraćnih infekcija (2007., nadopuna 2014.), ovaj je lijek prvi izbor za nekomplicirani cistitis odraslih žena zbog izvrsne učinkovitosti prema osjetljivim i ESBL rezistentnim sojevima E. coli te niskog potencijala za stvaranje rezistencije ("kolateralne štete"). Postoje, međutim, indicije kako učestala upotreba može dovesti do porasta rezistencije. Jedna studija provedena u Španjolskoj [4] zabilježila je porast infekcija uzrokovanih sojevima E. coli koji proizvode ESBL u devet bolnica između 2005. i 2009. te porast rezistencije na fosfomicin s 4,4 % na 11,4 %.
Podnošljivost lijeka slična je ostalima u ovoj skupini. Najčešće se susreću gastrointestinalni poremećaji (nadimanje, učestale rijetke stolice), glavobolja i vaginalni pruritus. U usporedbi s nitrofurantoinom, nuspojave su nešto rjeđe (6 % nasuprot 8 %), ali je incidencija pijelonefritisa nešto veća (2 % nasuprot 0,4 %).
Dozira se jednom dnevno, za žene iznad 50 kg 3 grama, 2 sata prije ili 2 sata nakon obroka. Nakon peroralne primjene apsorpcija je brza. Bioraspoloživost iznosi 30 – 37 %, ovisno o uzimanju neposredno nakon obroka ili kasnije. Ne metabolizira se u jetri, već se primarno izlučuje nepromijenjen bubrezima putem glomerularne filtracije. Vršne serumske koncentracije postižu se nakon 4 sata (3 grama), ali se u tragovima (100 mg/l) može dokazati u plazmi još 48 sati nakon uzimanja, zbog čega se ponavljajuće doze primjenjuju svaki drugi dan. Dobro prodire u tkiva urogenitalnog sustava (bubrezi, stijenka mokraćnog mjehura, prostata, sjemeni mjehurići), no koncentracije su nešto niže nego u urinu. Urinarne koncentracije manje su pri smanjenoj bubrežnoj funkciji pa se u pacijenata s niskim klirensima (CrCl 7 – 54 ml/min) koncentracija smanjuje s 32 % na 11 %. Baktericidni učinak ovisan je o vremenu (time-dependent killing), što znači da se optimalni učinak postiže kada je slobodna koncentracija lijeka iznad minimalne inhibitorne koncentracije (%fT > MIC) tijekom 40 – 50 % intervala doziranja.
Doziranje fosfomicina [5,6]
Pacijenti iznad 15 godina |
Pacijenti iznad 15 godina |
Pacijenti iznad 15 godina |
Djeca ˂ 15 god(CrCl ˃ 50 ml/min) |
Djeca ˂ 1 god(CrCl ˃ 50 ml/min) |
|
Dijagnoza |
CrCl ˃ 10 – 50 ml/min |
CrCl 10 – 50 ml/min |
CrCl ˂ 10 ml/min |
||
Nekomplicirani cistitis |
3 gr PO, 1 doza |
3 gr PO, 1 doza |
3 gr PO,1 doza |
2 gr PO,1 doza |
1 gr PO,1 doza |
Komplicirani cistitis |
3 gr PO, svaki II. dan7 – 21 dan |
3 gr PO, svaki III. dan7 – 21 dan |
3 gr PO, svaki III. dan7 – 21 dan |
2 gr PO, svaki II. dan7 – 21 dan |
1 gr PO, svaki II. dan7 – 21 dan |
Vrećicu s lijekom treba otvoriti i otopiti u 90 – 120 ml hladne vode te popiti 2 sata prije ili nakon jela. Duljina liječenja ovisi o vrsti i osjetljivosti uzročnika, odnosno potvrdi eradikacije mikrobiološkom pretragom urina.
Učinkovitost prema rezistentnim sojevima
U istraživanju Oua i sur. fosfomicin je pokazao visoku stopu učinkovitosti (96 %) prema 95 ESBL E. coli ili AmpC E. coli izolata u tri kanadske bolnice između 2015. i 2016. [7]. Mada je jednokratno doziranje za nekomplicirane cistitise i prema osjetljivim uzročnicima u brojnim studijama potvrđeno kao učinkovito i usporedivo s drugim standardnim lijekovima, u kompliciranim infekcijama te pogotovo u infekcijama uzrokovanim višestruko rezistentnim bakterijama ipak je nedovoljno. U ovim slučajevima preporučuju se tri doze svaki drugi ili treći dan tijekom 9 dana [8,9]. Učinkovitost fosfomicina kod cistitisa uzrokovanih rezistentnim uzročnicima procijenjena je u nekoliko nerandomiziranih studija. U retrospektivnoj studiji Neunera i sur. uključen je 41 pacijent s infekcijama uzrokovanim višestruko rezistentnim uzročnicima. Mikrobiološko izlječenje registrirano je u 59 % slučajeva, a u infekcija uzrokovanih E. coli koja proizvodi ESBL i K. pneumoniae u 70 % slučajeva [8]. U drugoj studiji s izolatima koji proizvode ESBL, kliničko poboljšanje i mikrobiološka eradikacija postignuti su u 94 % i 79 % slučajeva [9]. Ovi podaci potvrđuju značajan potencijal fosfomicina protiv višestruko rezistentnih sojeva, ali uz višekratnu primjenu. Učinkovitost prema P. aeruginosa i K. pneumoniae manja je u odnosu na ostale uropatogene. Prema E. coli, kao još uvijek najčešćem uzročniku (80 % cistitisa), neovisno o tome radi li se o osjetljivim ili višestruko rezistentnim sojevima, ima vrlo dobar antibakterijski učinak, ali je i ovdje potreban oprez jer prečesta primjena može inducirati rezistenciju. Ovo pravilo vrijedi, uostalom, za sve antibiotike.
Rezistencija na fosfomicin prvenstveno je kromosomska, no u zadnje vrijeme bilježi se pojava izolata s plazmidnim tipom rezistencije. Kromosomska rezistencija nastaje kao posljedica spontanih mutacija koje interferiraju s dva bakterijska transportna sustava potrebna za aktivni prijenos lijeka u stanicu, zbog čega su međustanične koncentracije znatno smanjene. Ovaj tip rezistencije susreće se relativno rijetko i nije udružen s rezistencijom na druge antibiotike. Plazmidna rezistencija kodirana je dvama genima: FosA i FosB. FosA je glutation-S-transferaza koja se veže s fosfomicinom u inaktivni konjugat. Opisana je samo u gram-negativnih bakterija. Gram-pozitivne bakterije, najčešće Staphylococcus spp. nose FosB gene, no točan mehanizam inaktiviranja fosfomicina još nije razjašnjen.
Literatura:
1. Chakraborty AK, Muneim GE, Pradhan S, et al. Superbug horror and its relations to antibiotics, probiotics and vitamins. J Pharm Toxicol. 2018;1(1):14-9.
2. Levine DP. Vancomycin: A history. Clinical Infectious Diseases 2006; 42:S5–12
3. Falagas ME et al. J. Antimicrob. Chemother. 2010; 65: 1862-77
4. Oteo J. et al. J. Antimicrob. Chemother. 2010; 65: 2459-63
5. Paul A. Pham, John G. Bartlett. Fosfomycin. Available at http://hopkinsabxguide.org/antibiotics/antibacterial/misc/fosfomycin
6. Falagas ME, Vouloumanou EK, Togias AG, et al. Fosfomycin versus other antibiotics for the treatment of cystitis: a meta-analysis ofrandomized controlled trials. J Antimicrob Chemother. 2010; 65: 1862-77
7. Ou LB, Nadeau L. Fosfomycin susceptibility in multidrug-resistant Enterobacteriaceae species and vancomycin-resistant Enterococci urinary isolates. Can J Hosp Pharm. 2017;70(5):368-374.
8. Neuner EA, Sekers J, Hall GS, van Duin D. Experience with fosfomycin for treatment of urinary tract infections due to multidrug-resistant organisms. Antimicrob Agents Chemother. 2012;56(11):5744-5748. doi: 10.1128/AAC.00402-12.
9. Pullukcu H, Tasbakan M, Sipahi OR, Yamazhan T, Aydemir S, Ulusoy S. Fosfomycin in the treatment of extended spectrum beta-lactamase-producing Escherichia coli-related lower urinary tract infections. Int J Antimicrob Agents. 2007;29(1):62-65. doi: 10.1016/j.ijantimicag.2006.08.039.



